Contexte

Les biofilms sont des communautés microbiennes denses associées entre elles ou à des surfaces et enrobées par une matrice extra-cellulaire qui les protège (Figure 1).
Présents dans tous les environnements naturels, les biofilms peuvent aussi être responsables d’infections chez l’Homme (Figure 2).
Enjeu

Les biofilms bactéries constituent une complication de l’usage des dispositifs médicaux implantés, comme les cathéters vasculaires, urinaires ou bien les matériaux implantés lors de chirurgie orthopédiques, comme les prothèses articulaires (Figure 2).
L’enjeu est majeur car lorsque les bactéries forment des biofilms, elles sont plus difficiles à éradiquer par des antibiotiques.
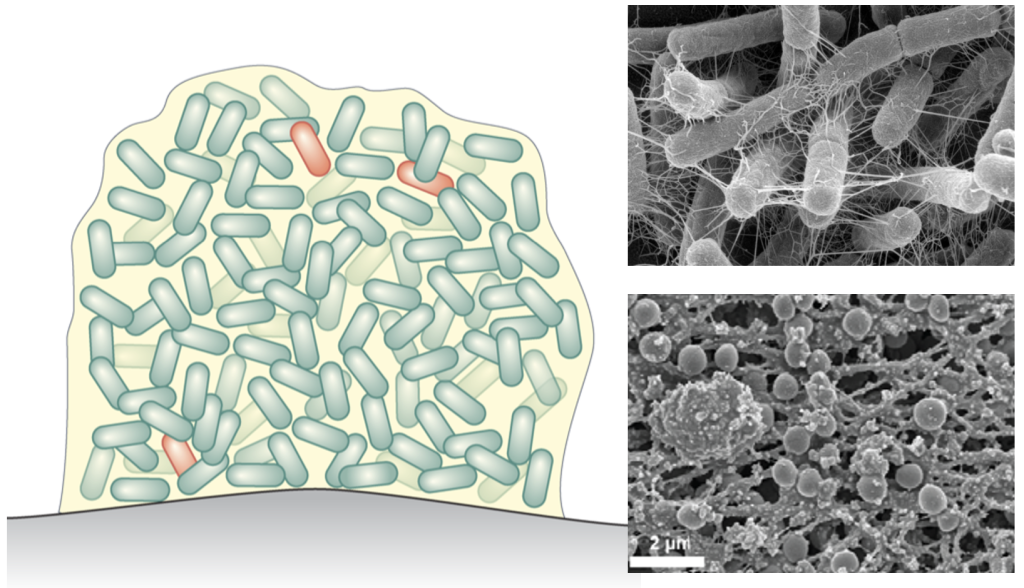
Figure 1
Travaux menés
La première étape de ce travail de recherche sera de préciser où se développent les biofilms en cas d’infection sur prothèse articulaire.
Les chercheurs vont analyser la zone se trouvant entre la prothèse articulaire et l’os (membrane d’interface) afin d’essayer d’y détecter la présence de biofilms.
Pour cela, ils vont utiliser des techniques de microscopie électronique (Figure 1) ou de fluorescence, permettant de voir des bactéries et ainsi les distinguer d’autres éléments présents à côté de la prothèse (cellule immunitaire, cellule osseuse…).
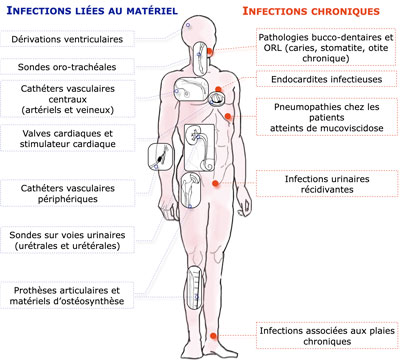
Figure 2
Les chercheurs du groupe de travail

Christophe BELOIN

Jean-Marc GHIGO

David LEBEAUX
Pour aller plus loin
L’objectif de ce projet est de rechercher et caractériser les biofilms bactériens au niveau de la membrane d’interface entre la prothèse articulaire et l’os mais également au niveau des pièces mobiles de prothèses articulaires.
Les prélèvements seront réalisés par le chirurgien orthopédique chez des patients ayant une infection sur prothèse articulaire et nécessitant une reprise opératoire avec ablation de la prothèse.
Des témoins seront inclus : patients nécessitant un changement de prothèse articulaire du fait d’un descellement aseptique. Les chirurgiens prélèveront des fragments de membrane d’interface mais également les pièces mobiles de la prothèse.
Pour identifier les biofilms, la microscopie électronique à balayage permettra d’analyser la surface de la membrane d’interface et la microscopie électronique a transmission permettra d’étudier la membrane dans son épaisseur. Enfin, la microscopie confocale à fluorescence sera utilisée pour distinguer les biofilms d’autres structures non bactériennes grâce à l’usage de sondes ciblant spécifiquement une espèce bactérienne (FISH).
Le projet a reçu l’accord du comité d’éthique de l’Institut Pasteur, et est l’objet d’une demande de financement.
Si ces données préliminaires confirment la présence de biofilms, une étude cas-témoin sera mise en place pour évaluer spécifiquement l’influence de ces biofilms dans le risque d’échec thérapeutique en cas d’infection sur prothèse articulaire.





